Nathan Cruz
Você já pensou que o computador que você utiliza hoje para ler o nosso blog, os seus e-mails, as últimas notícias do mundo são frutos de um pesquisa científica, ou seja uma idéia que nasce de uma pergunta, ou de uma hipótese – academicamente falando.
A idéia e sua produção como afirmação da pesquisadora Moroz (2002) surge de uma representação da vida do ser humano, ou seja em dado momento essa idéia reflete a vontade de buscar o conhecimento para o enriquecimento de sua história ou contexto social.

A World Wide Web, ou a tão utiliza da internet surgiu das necessidades células militares comunicarem-se entre si em locais distantes, em diferentes países durante o pós-guerra.
O contexto social, a necessidade diária fez com que um grupo de pesquisadores buscassem um forma de comunicação através de tentativas e erros calculados, até o produto final. Na foto ao lado temos a impressão de estar vendo uma foto da NASA, de alguma galáxia, pelo contrário esta é uma esquematização gráfica da mundial de computadores interligados entre si, e você que está lendo este blog está em algum deste ponto. E tudo isso foi graças a ciência.
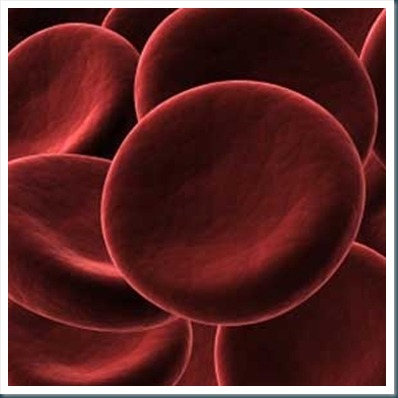
 Um exemplo mais próximo da nossa realidade é o tubo de micro-hematócrito, também chamado de microcapilar, pois é o conceito que os líquidos passam dentro de cilindros bem espessos vem das pesquisas físicas de Albert Einstein. A pesquisa dele foi aplicada na medicina que na época não existia a especialização hematologia, no entanto começaram a avaliar o sangue para utilização na transfusão em fronts, onde avaliação hemácia e o hematócrito. Mais uma vez um conceito de hipótese, necessidade e aplicação.
Um exemplo mais próximo da nossa realidade é o tubo de micro-hematócrito, também chamado de microcapilar, pois é o conceito que os líquidos passam dentro de cilindros bem espessos vem das pesquisas físicas de Albert Einstein. A pesquisa dele foi aplicada na medicina que na época não existia a especialização hematologia, no entanto começaram a avaliar o sangue para utilização na transfusão em fronts, onde avaliação hemácia e o hematócrito. Mais uma vez um conceito de hipótese, necessidade e aplicação.
Será que o Einstein foi até o laboratório da época e falou – Ou cumpadi passa o sangue nesse tubo acho que vai servir! – ou então – O cara do laboratório bateu lá na porta do Einstein – Dá licença seu Einstein, belê? Oww… estávamos precisando uma idéia para quantificar quando de sangue indivíduo tem, e desta forma criar uma forma saber quando ele precisa de sangue, tipo assim tô tentando avaliar volume globular, o senhor tem alguma idéia!
Bem não foi assim, hoje até poderia ser – Nossa Einstein, genial RELATIVIDADE publica no facebook - mas antes no “século passado”, sem os adventos da internet, os cientistas ficavam isolados e a comunicação de suas idéias era feita pelos jornais, mas principalmente através de comunicações técnicas, que eram passadas através dos pesquisadores daquele determinado nicho científico. Somente assim cada um sabia o que o outro estava fazendo – a transmissão de idéias … por escrito é uma das características que o ser humano foi adquirindo, uma forma de acumular o conhecimento: a produção científica é um processo de construção do qual fazem parte os conhecimentos anteriormente formulados.
Conforme abordado por Moroz (2002), “não pretende-se acumular conhecimento de forma linear: a acumulação não é apenas a incorporação constante do anteriormente produzido, mas pode ser também a negação do conhecimento até então aceito. Quando uma nova forma de explica a realidade passa a vigorar, tornando a anterior inadequada”.
De tudo que falamos até agora podemos enxergar a importância do artigo científico, também chamado de paper. O paper comunica a sociedade científica daquele determinado nicho científico a pesquisa, por exemplo:
Dárcio é veterinário hematologista de vaca de leite, e um dia trabalhando leitura de reticulócitos utilizando azul de metileno começou a ficar insatisfeito, depois de tentar várias diluições deste corante, ele utilizou tinta nanquim azul e viu que o esfregaço ficou mais limpo, sem resíduos de corante. Então ele resolveu contar para todo mundo desta técnica coloração. Então ele escreveu um comunicado para os interessados em vaca de leite (1º nicho), mais especificamente aqueles que trabalham hematologia (2º nicho), que facilitou a vida dele e denominando-a de Coloração Dárcio.
A primeira coisa que ele procurou foi uma revista, e escolheu a Conhecimento Veterinária. Mas seu colega chamado Luciano, falou que está revista não estaria a altura de sua descoberta e que ele deveria publicar um periódico (sinônimo = revista), já que a Conhecimento era um “revista” simples e que lá sua pesquisa não teria um “fator de impacto” como deveria. Daí o Dárcio pensou nossa o qual a diferencia de periódico e revista, e o que significa fator de impacto.
 REVISTA X PERIÓDICO - Bem revista e período são ambos meios de comunicação escrita, em que a informação deixa de ser privada, individual e passa a torna-se pública. No entanto, o Luciano referiu-se a revista como sendo algo de segunda mão. Pelo contrário o que ele falou é que a revista, neste caso a Conhecimento Veterinária tem um cunho voltada para um público em geral, mais popular, com linguagem fácil, cheia de variedades, sem termos muitos técnicos e conceitos menos elaborados.
REVISTA X PERIÓDICO - Bem revista e período são ambos meios de comunicação escrita, em que a informação deixa de ser privada, individual e passa a torna-se pública. No entanto, o Luciano referiu-se a revista como sendo algo de segunda mão. Pelo contrário o que ele falou é que a revista, neste caso a Conhecimento Veterinária tem um cunho voltada para um público em geral, mais popular, com linguagem fácil, cheia de variedades, sem termos muitos técnicos e conceitos menos elaborados.
Já um periódico é uma publicação voltada para público muito mais específico, editada com regularidade temporal maior que a revista, com menos ou nenhuma propaganda, termos e conceitos técnicos que instiguem no leitor a vontade comentar, discutir, a argumentar as informações que estão sendo mostradas. Os periódicos podem também ser chamados de revista científica é tem como intuito maior divulgar os progressos da ciência, e tem artigos que foram revisados por pares, com objetivo de assegurar a validade dos dados citados, sendo suficiente para suprir que caso um pesquisador independente queira repetir aquele experimento informado, possa verificar resultados semelhantes ou próximos dos citados, tornando aquela revista como um registro permanente da produção científica daquela área.
argumentar as informações que estão sendo mostradas. Os periódicos podem também ser chamados de revista científica é tem como intuito maior divulgar os progressos da ciência, e tem artigos que foram revisados por pares, com objetivo de assegurar a validade dos dados citados, sendo suficiente para suprir que caso um pesquisador independente queira repetir aquele experimento informado, possa verificar resultados semelhantes ou próximos dos citados, tornando aquela revista como um registro permanente da produção científica daquela área.
FATOR DE IMPACTO - Com facilidades da internet, o mundo esta cada vez mais dentro de nossa casa, e temos acesso a todos “papers” e a veracidade e a qualidade das informações prestadas na revista científica devem ser imprescindível, e isso vai de encontro com o que o Luciano falou a respeito de fator de impacto. O fator de impacto é uma avaliação destes periódicos, sendo realizado por um órgão isento que comunica a mostra a comunidade científica a qualidade de trabalho de cada revista, no frigir podemos dizer que quanto maior for o fator maior será a leitura e a aceitação das informações como verdadeiras.
QUALIS é o sistema de avaliação brasileiro mantido pelo o CAPES – Coordenação de Aperfeiçoamento de Pessoal de Nível Superior do Ministério da Educação. O Qualis é o conjunto de procedimentos utilizados pela Capes para estratificação da qualidade da produção intelectual dos programas de pós-graduação. Tal processo foi concebido para atender as necessidades específicas do sistema de avaliação e é baseado nas informações fornecidas por meio do aplicativo Coleta de Dados. Como resultado, disponibiliza uma lista com a classificação de periódicos e anais de eventos utilizados pelos programas de pós-graduação para a divulgação da sua produção.
A estratificação desta classificação é baseado no cruzamento de várias informações deste o local (nacional e internacional) e qualifica no seguinte ranque – A, B e C sem que a escala é formada por oito estratos (A1, A2, B1 a B5 e C), sendo o estrato C de peso zero.
Munidos com estas informações Dárcio, procurou o periódico Vet Research Papers Lab., que tem um linha editorial voltadas para técnicas laboratoriais utilizadas em veterinária e tem um fator de impacto A2. A consultado dos fatores de impactos dos periódicos pode ser realizado gratuitamente no site do WEBQUALIS (http://qualis.capes.gov.br/webqualis/ConsultaPeriodicos.faces).
Definida o periódico, bastou apenas o Dárcio entrar no site da editora que o publica é ver as normas de publicação. Geralmente a estruturação dos artigos são feitas da seguinte forma:
TEMA – É importante esclarecer que um artigo científico não resume-se apenas a comunicação de resultados de uma pesquisa. Um paper pode ser um relato de caso, uma revisão de literatura, um comunicado sanitário. Enfim todo e qualquer tema que tenha importância científica e mereça ser comunicado para sociedade científica daquele determinado assunto.
RESUMO – Como o nome diz é uma explicação sucinta de todo estudo, isso facilita duas coisas para o leitor: 1º – Ele não precisa ler o trabalho inteiro para saber sobre o aquela pesquisa comenta. 2º – Papers são pagos e o preço é pouco salgado para ter-se acesso a todo conteúdo da pesquisa (FULL TEXT, denominação usual). Imagina pagar vinte dólares por um artigo e ele não servir. Então, as instituições de ensino superior para facilitar a vida dos pesquisadores, compram da editora uma licença de uso que é chamada de site licenses – permitindo assim qualquer acesso nas bases de uma determinada editora. Na UNIUBE temos a licença para maioria dos artigos da Science Direct (http://www.sciencedirect.com), nos computadores da universidade e de seus setores exceto do LIAE. Sempre é escrito na língua materna do autor.
ABSTRACT ou SUMMARY – Resumo em língua inglesa.
KEYWORDS ou Palavras-chaves – Este item facilita a vida das editoras e os agentes de biblioteconomia na hora de cadastrar o artigo e achar novamente – chamamos esta técnica de indexação, que facilita na recuperação daquele artigo em banco de dados, por exemplo dentro de uma biblioteca que tem um acervo de 20 mil periódicos e inúmeros papers. Vamos utilizar nosso exemplo, o artigo do Dárcio precisa ser indexado e o assunto de é sobre Utilização de tinta nanquim para determinação de reticulócitos em esfregaço sanguíneos de vacas leiteiras:
O artigo do Dárcio está pode ser classificado da seguinte forma – Ciências da Saúde: Medicina Veterinária: Hematologia: Eritrograma: Ruminantes: Bovinos Leiteiros: Técnicas Laboratoriais.
A indexação sempre tentará simplificar ao máximo a especialização do estudo do Dárcio, para ficar mais fácil quando precisarmos localizar em uma segunda oportunidade.
INTRODUÇÃO – Revisão bibliográfica que embase a pesquisa e o objetivo da pesquisa – Lembra-se o ato de pesquisa é pegar os conhecimentos já conhecidos e descobrir sua utilização ou então contesta-los.
MATERIAIS E MÉTODOS – Neste ponto o autor(es) irão contar tudo o que foi preciso para desenvolver tal pesquisa. Revistas que tem FI mais alto, exigem que autor descreva mais detalhadamente separando até por tópicos ex: Animais – Ambiente – Estatísticas – Formas de coleta dos dados e etc.
RESULTADOS E DISCUSSÃO – Aqui o autor(es) irão apresentar os resultados e discuti-los em relação a literatura existente. Em periódicos com FI mais alto tem-se a exigência de separar os resultados da discussão. Sendo assim, os resultados serão apresentados com tabelas e sua viabilidade estatística que comprova que aqueles dados apresentaram diferença e são relevantes, quando compara-se um grupo controle do testado. Na discussão serão abordados apenas os dados significantes com a argumentação pertinentes para eles. Tanto no resultados ou na discussão pode ser anexadas fotos do experimento, das amostras, gráfico e dentro outros elementos que ilustrem tal trabalho científico.
CONCLUSÃO – É a finalização do artigo e traz em suma as conclusões do pesquisador quanto a sua pesquisa, como que pode-se afirmar que os resultados significantes a respeito da determinado experimento inferem que a administrar cloranfenicol para cães por longo período causa aplasia medular, por exemplo.
REFERÊNCIAS – Parte dedicada as referências utilizadas para construção do paper, sendo que a referência bibliográfica é o conjunto de elementos de uma obra escrita que permite a identificação por qualquer pessoa.
EXERCÍCIO
Bem já que conhecemos o que é um paper, e suas características vamos fazer o seguinte exercício:
A) Escrever um artigo científico com o seguinte título: Caracterização dos leucócitos totais e respectiva importância clínica de veterinária – revisão de literatura.
B) Escolher uma periódico e montar o seu artigo nas normas dele, escolher o periódico no Science Direct, Scielo – Lembre-se mostrar qual o nome, o fator de impacto e do endereço da homepage da publicação.
C) O artigo poderá ser escritos em grupo de até quatro pessoas.
DICA: Lembre-se de escrever sobre todas as espécies animais, já que o artigo servirá como fonte de estudo para a 2º Prova de Diagnóstico Laboratorial. E que teremos sempre todas as semanas dicas para confeccionar este trabalho.
ENTREGA – Até 15 de outubro através do e-mail nathancruz@live.com
Referências deste post
MOROZ, M; GIANFALDONI, M. H. T. A. O processo de pesquisa: iniciação. Plano: Brasília, 2002.
Fator de impacto - http://www.ib.unicamp.br/biblioteca/fator
Webqualis - http://qualis.capes.gov.br/webqualis/ConsultaPeriodicos.faces





![clip_image002[4] clip_image002[4]](https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEjFxQPm-zUiGtK_iQlVpCCYSoHsv4j1ukBmy1DKpxTCrY1NDzRuoAFPKmi0eduaX-cggfrOmJ4LRepfempMSUgl0Qm_WgXQv8WySRgxctjG4UhgBms41_GRiw2ruJwfxMG9Ed_X09WqDhr8/?imgmax=800)



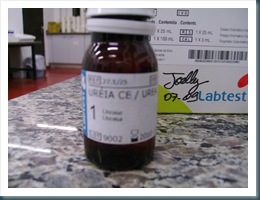
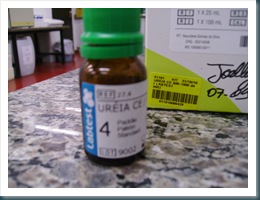
 Fig. 1. Kit Uréia CE Labtest.
Fig. 1. Kit Uréia CE Labtest. 





 Na prova de TP o cronômetro é o principal instrumento pois através dele que iremos mensurar o tempo da coagulação do plasma citratado.
Na prova de TP o cronômetro é o principal instrumento pois através dele que iremos mensurar o tempo da coagulação do plasma citratado.
 Alça de Drygalsk ou também alça de platina é necessária para confirmar e segurar o coágulo presente no tubo.
Alça de Drygalsk ou também alça de platina é necessária para confirmar e segurar o coágulo presente no tubo.
 Fig. 2. Cascata de coagulação, evidenciando somente a participação da protrombina.
Fig. 2. Cascata de coagulação, evidenciando somente a participação da protrombina.
 RISCO BIOLÓGICO: Produtos (organismos ou substâncias) que representam risco a saúde humana. Constituem risco biológico o lixo hospitalar, sangue, amostras de microrganismos
RISCO BIOLÓGICO: Produtos (organismos ou substâncias) que representam risco a saúde humana. Constituem risco biológico o lixo hospitalar, sangue, amostras de microrganismos



 Produto Perigoso para o Meio Ambiente: produtos com este símbolo podem contaminar o meio ambiente. Guardar estes produtos em recipientes adequados e nunca derramar para o meio ambiente.
Produto Perigoso para o Meio Ambiente: produtos com este símbolo podem contaminar o meio ambiente. Guardar estes produtos em recipientes adequados e nunca derramar para o meio ambiente.