1) Podemos descobrir os valores de Hemoglobina e Hemácias à partir do Hematócrito dividindo por 3 e por 6, respectivamente. Porque isso não é aconselhável?
R: Porque podemos ter um índice falso já que nivelamos os níveis de Hg e He ao valor do hematócrito correspondente, obtendo por muita das vezes valores de normalidade.
2) O que é hematócrito e como ele é dividido?
R: Segundo Samuelson (2007) Hematócrito é os elementos figurados do sangue tratados previamente com anticoagulante e centrifugados, que formam as duas camadas mais baixas no tubo, sendo a camada mais baixa, maior, viscosa e vermelha, composta pelas células vermelhas do sangue. A camada intermediária chamada de camada leucocitária, ou buffy coat, de espessura fina e de cor branca acinzentada, compostas pelas células brancas e pelas plaquetas, representando, aproximadamente 1% do volume total de sangue. O plasma compõe a última camada, o qual tem coloração amarelada, e que compreende 55 – 60% do volume total do sangue (Fig. 1).
Fig. 1 – Ilustração de sangue com anticoagulante que foi separado por centrifugação em três camadas.
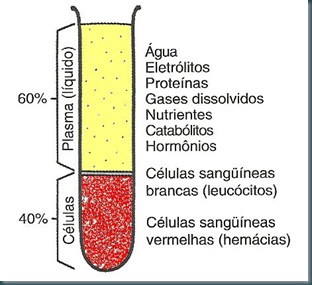 FONTE: SAMUELSON, D. A. Tratado de histologia veterinária. cap. 7. p. 125-126. fig. 7-1. ELSEVIER: Rio de Janeiro, 2007.
FONTE: SAMUELSON, D. A. Tratado de histologia veterinária. cap. 7. p. 125-126. fig. 7-1. ELSEVIER: Rio de Janeiro, 2007.
3) Qual a influência das catecolaminas nos aumentos dos valores de hematócrito e hemoglobina?
R: As catecolaminas causam uma contração esplênica, injetando um volume concentrado de hematócrito na circulação periférica, tendo uma influência direta sobre o hematócrito. Quanto a hemoglobina, o efeito é indireto já que sua concentração e a contagem de hemácias são padronizadas ao valor do hematócrito, são paralelo dependentes a influência das catecolaminas (MEYER et al, 1995).
4) Qual é o fator sérico para produção de hemácias no sangue?
R: O fator sérico é a baixa concentração de O2 ou a alta concentração de CO2 que estimulam a liberação de eritropoietina fisiologicamente apropriado. Um exemplo disso é quando o organismo sofre com uma doença pulmonar que prejudica a troca gasosa, ou quando o organismo é fica em condições de baixa concentração de O2 atmosférico.
5) Defina:
a) reticulócitos: São hemácias jovens anucleadas, com a presença de uma malha reticular, de RNA ribossômico, mecanismos de síntese protéica, incluindo ribossomos, retículo endoplasmático rugoso (RER) e mitocôndrias. Em certos casos de atividade eritropoética aumentada, tais células são observadas com maior frequência e podem servir como um indicador do aumento na produção de hemácias. Não encontrados em equinos, ovinos, caprinos e bovinos saudáveis. Em gatos e cães, no em quantidade de 0,5 a 1,0% podem estar presentes, e em 2% nos suínos.
 FONTE: Ciência News (2010).
FONTE: Ciência News (2010).
b) policitemia: Consiste no aumento da massa de eritrócitos, hemoglobina e hematócrito, acompanhado de um aumento do volume sangüíneo total. O quadro deve ser diferenciado da eritrocitose secundária à perda ou baixa ingestão de líquidos ou a um estímulo mieloproliferativo.
 FONTE: Ciência News (2010).
FONTE: Ciência News (2010).
c) anisocitose: variação no tamanho dos eritrócitos (heterogeneidade).
 FONTE: WEB ARTIGOS (2010).
FONTE: WEB ARTIGOS (2010).
d) policromasia: variação na coloração dos eritrócitos num mesmo esfregaço de sangue.
 FONTE: Portal Veterinária (2009).
FONTE: Portal Veterinária (2009).
6) Para cada tipo de exame utilizamos um tipo de tubo que tem tampa e conteúdo diferentes, então determine o uso e conteúdo de cada tubo:
a) tampa amarela: Tubo com gel separador e ativador de coágulo que serve para exames bioquímicos e sorológicos.
b) tampa vermelha: Sem anticoagulante, serva para análises ao soro sanguíneo sendo utilizados para provas sorológicas e bioquímicas.
c) tampa roxa: Possui EDTA, que sequestra o Ca e impede a coagulação é utilizado para hematologia. Quando o tubo possui gel separador é utilizado para exames de carga viral.
d) tampa azul: Possui citrato de sódio, que capta íons de Ca. Serve para estudos de coagulação sanguínea.






e) tampa verde: Possui Heparina, que pode ser sódica ou lítica, ambas evitam a coagulação do sangue serve para exames toxicológicos.
f) tampa cinza: Tem Fluoreto de Sódio com EDTA, serve para exames que visão dosar a glicose sérica. O EDTA possui poder anticoagulante e o Fluoreto de Sódio impede a utilização da glicose pelos elementos figurativos do sangue.
7) Quando o organismo animal se apresenta em hipóxia aguda causa que tipo de alteração hematológica para reverter o problema?
R: O organismo aumenta a produção de hemácias através da liberação de eritropoietina.
8) Os eritroblastos reticulócitos e o VCM aumentados são parâmetros importantes para a classificação da anemia quanto a resposta medular. Baseado nesse comentário do monitor Willer, explique fisiologicamente o que são reticulócitos e eritroblastos e estabeleça uma correlação fisiológica entre essas células e a resposta medular para cães e cavalos.
R: Os eritroblastos, também chamados de rubrícito, são células percursoras de eritrócitos, que possuem o citoplasma rosa ou avermelhado, podendo ser ligeiramente policromático, rodeando um núcleo picnótico (citologia: quando o núcleo apresenta cromatina extremamente condensada, podendo também indicar uma necrose tecidual) e escuro. Os eritroblastos quando excluem o núcleo passam a ser chamados de reticulócitos que são células anucleadas e possuem algumas organelas, além do arranjo da hemoglobina, no entanto a troca gasosa é por muitas das vezes deficitárias. Nos casos dos canídeos a presença de até 1% de reticulócitos não caracteriza problemas na eritropoese, enquanto que em cavalos essa células indica alterações na resposta medular. Em ambas as espécies a presença de eritroblasto pode indicar severidade na perca de sangue ou distúrbio mieloproliferativo.
9) Classifique os eritrogramas:
a) Cão, hemácias: 3.75 mm³, Hematócrito: 25,8%, Hemoglobina: 8,4 g/dL, VCM: 68,8 fl, HCM: 22,5 pg e CHCM: 32,5 g/dL. Anemia Normocítica Normocrômica. Não-regenerativa.
MOTIVO: Depressão da eritrogênese por inflamação crônica, insuficiência renal crônica ou hipoplasia medular.
b) Gato, hemácias: 4,85 mm³, Hematócrito: 18%, Hemoglobina: 6,5 g/dL, VCM: 37,1 fl, HCM: 13,4 pg e CHCM: 36,1 g/dL. Anemia Normocítica Normocrômica. Não-regenerativa.
MOTIVO: Depressão da eritrogênese por inflamação crônica, leucemia vírus felino ou hipoplasia medular.
c) Bovino, hemácias: 3,25 mm³, Hematócrito: 27%, Hemoglobina: 9,8 g/dL, VCM: 83,07 fl, HCM: 30,15 pg e CHCM: 36,29 g/dL Anemia Macrocítica Normocrômico (Hipercrômico aterfato). Pouco Responsiva, regenerativo.
MOTIVO: Deficiência de cobalto.
d) Equino, hemácias: 9,2 mm³, Hematócrito: 38%, Hemoglobina: 14 g/dL, Fib: 400 mg/dL VCM: 41,30 fl, HCM: 15,21 pg e CHCM: 36,84 g/dL Sem anemia. Normocrômico (Hipercrômico por artefato).
MOTIVO: Possível hemólise ou lipemia que mascaram o resultado.
Observação: Há no bovino e no equino, um CHCM alto, o que índica hipercrômia dos eritrócitos, isso é considerado um artefato pois, o que confere cor a estas células é o composto heme que se liga ao um átomo de ferro, sendo fisiologicamente impossível o eritrócito produzir mais hemoglobina no seu interior, então o CHCM maior que nível máximo de referência é fisiologicamente impossível, então podemos considerar que em ambos casos há um Hb livre que contribui para alterações na espectrofotometria (MEYER, 1995). Ravel (1997) além da teoria de Hb livre justifica que pode estar acontecendo um esferocitose (anemia microcítica hipercrômica hereditária, em que as hemácias se apresentam pequenas e hipercoradas), lipemias graves, aglutininas (glicoproteínas sanguínea produzidas pelo aglutinogênio que é responsável pela fenotipagem sanguínea) e em casos de fumantes inveterados (humanos).
10) As policitemias é caracterizada quando os valores hematimétricos estão acima do normal. Quais tipos de policitemias existentes e quais suas principais causas?
Policitemia Absoluta: Aumento do número total de células, esta eritrocitose pode ser ocasionada há uma deficiência da saturação de O2 (devido a pressão atmosférica ou defeitos na ventilação pulmonar), transtornos circulatórios e em recém nascidos.
Policitemia transitória: Redistribuição eritrocitária na circulação (contração do baço) causadas por exercícios, diminuição do oxigênio, emoção e hemorragias agudas.
Policetemia relativa: É causada pela hemoconcentração, devido a ingestão diminuídas de líquido, perdas de água (desidratação), vômitos, diarréia, equinos que apresentem cólicas e tétano e em casos de choque.

 FIG. 4 – Resultados do ABC Vet FONTE: SCIL (2010).
FIG. 4 – Resultados do ABC Vet FONTE: SCIL (2010).










 O Prof.. Rodrigo Supranzetti atendeu uma cadela, chamada Babi, que pesava 6 Kg, sendo da raça fox paulistinha, com 168 meses. Na anamnese o paciente não estava se alimentando em um período de 2 a 3 dias, tinha tomado dipirona e não apresentou nem vômito e diarréia. Sua alimentação é composta por comida e ração, a vacinação está em dia e a vermifugação foi realizada a 4 meses. Babi mora com mais dois animais que não apresentaram nenhuma sintomatologia.
O Prof.. Rodrigo Supranzetti atendeu uma cadela, chamada Babi, que pesava 6 Kg, sendo da raça fox paulistinha, com 168 meses. Na anamnese o paciente não estava se alimentando em um período de 2 a 3 dias, tinha tomado dipirona e não apresentou nem vômito e diarréia. Sua alimentação é composta por comida e ração, a vacinação está em dia e a vermifugação foi realizada a 4 meses. Babi mora com mais dois animais que não apresentaram nenhuma sintomatologia.